Sleep, 18(3):167-171.
1995, Американская Ассоциация Расстройств сна и Общество по исследованиям сна.
Yoshihiro Yamashiro and Meir H. Kryger.
Отдел респираторной медицины, Университет г. Манитоба, Канада.
Резюме: цель настоящего исследования заключалась в том, чтобы изучить диагностическую ценность проводимой в домашних условиях оксиметрии при скрининге расстройств сна у пациентов, предъявляющих жалобы на избыточную дневную сонливость (ИДС).
Для решения поставленной задачи проводилось слепое сравнительное исследование диагнозов, поставленных при помощи изолированной оксиметрии и диагнозов, поставленных при помощи полисомнографии, проведенной в сомнологическом центре больницы.
В исследование были включены 300 пациентов, направленных всвязи с наличием избыточной дневной сонливости с подозрением на наличие апноэ сна. Был осуществлен целый ряд исследований. Информация об уровне насыщения крови кислородом (Sa02) записывалась с частотой 2 Гц и сохранялась в цифровом виде во время полисомнографии. На основании анализа данных Sa02, записанных на бумагу, 6 специалистов рассчитывали количество событий десатурации > 3% за час (индекс десатурации — ИД) и формулировали диагноз (норма – ИД < 5; обструктивное апноэ сна легкой степени – 5 < ИД < 20; обструктивное апноэ сна средней тяжести – 20 < ИД < 40; обструктивное апноэ сна тяжелой степени – ИД > 40). Синдром повышенной резистентности верхних дыхательных путей диагностировался в том случае, когда ИД был < 5 событий в час, и сочетался с незначительными флуктуациями уровня Sa02.
Диагнозы, поставленные каждым из шести анализировавших запись специалистов, сравнивались с клиническими диагнозами, поставленными на основании независимого анализа полисомнографических записей. 31 запись (10,3%) были исключены подсчитывающими специалистами из-за неадекватности сигналов Sa02, потребовавших вмешательства технолога. Чувствительность метода (оксиметрии) для скрининга нарушений дыхания во сне составила 90%, а специфичность – 75%. Все пациенты с ОАС тяжелой и средней степени были выявлены при помощи оксиметрии. Вместе с тем, из 66 пациентов, которые по данным оксиметрии были признаны «здоровыми», у 1-го имелось обструктивное апноэ сна легкой степени, у 20-ти – синдром повышенной резистентности верхних дыхательных путей, у 9-ти периодические движения конечностей во время сна, у 4-х нарколепсия и у 2-х парасомнии. Таким образом, оксиметрия, проведенная а амбулаторных условиях, может не обладать достаточной чувствительностью и специфичностью для надежного выявления нарушений дыхания во время сна, и является бесполезной для выявления других расстройств сна.
Избыточная дневная сонливость (ИДС) является наиболее распространенным симптомом, являющимся показанием для направления пациента в лабораторию сна. Наиболее частой причиной ИДС являются нарушения дыхания во время сна. Эти расстройства широко распространены среди населения и связаны с существенной заболеваемостью и повышенной смертностью; при этом они хорошо поддаются специфическому лечению. Поэтому, эффективная и экономичная скрининговая система могла бы представлять существенную ценность. В настоящее время продолжаются дискуссии относительно применения с этой целью домашней (амбулаторной) оксиметрии.
Результаты ряда исследований свидетельствуют о том, что домашняя оксиметрия является полезной для выявления обструктивного апноэ сна (ОАС). Вместе с тем, диагностическая значимость изолированной оксиметрии при обследовании пациентов с избыточной дневной сонливостью, у которых предполагается наличие нарушений дыхания во время сна, остается неясной. В частности, не определена роль оксиметрии для диагностики синдрома повышенной резистентности верхних дыхательных путей (СПРВДП). СПРВДП также вызывает избыточную дневную сонливость и часто хорошо поддается лечению. Кроме того, у некоторых пациентов, у которых подозревается наличие нарушений дыхания во время сна, могут иметь место и другие расстройства сна. В настоящем исследовании нами проведен сравнительный анализ диагностической значимости полного ночного полисомнографического исследования и изолированной оксиметрии при обследовании пациентов, направленных лечащими врачами в сомнологическую лабораторию с подозрением на наличие нарушений дыхания во сне.
Материалы и методы
Триста пациентов (211 мужчин и 89 женщин, средний возраст – 47.0+13.4 лет), обследованных при помощи ночного полисомнографического исследования (ПСГ) в нашей лаборатории были рандомизированы для данного ретроспективного исследования. Пациенты были направлены в лабораторию в связи с наличием у них избыточной сонливости и с подозрением на наличие нарушений дыхания во сне. ПСГ-исследование включало регистрацию электроэнцефалограммы (С4/А1, О1/А2), электроокулограммы, подбородочной электромиограммы (ЭМГ), ЭМГ в передней большеберцовой мышцы, электрокардиограммы, движений грудной клетки и мышц живота (при помощи респираторной индуктивной плетизмографии), ороназального воздушного потока при помощи анализатора С02 (Datex Normocap 200). Насыщение кислородом артериальной крови (Sa02) мониторировалось при помощи оксиметра (Biox 3740) с использование ушного датчика; сигнал записывался как максимально быстрый ответ (3 секунды) при помощи полиграфа (Grass 78E).
Сигнал также оцифровывался и записывался в компьютер с частотой 2 образца в секунду (2Гц). На основании данных, записанных на диске в отдельном файле, на бумаге изображалась кривая, представляющая значения Sa02 со скоростью 2 дюйма (1 дюйм = 25,4 мм) в минуту.
При постановке клинического диагноза СПРВДП на основании анализа ПСГ-записей мы применяли критерии, связанные с выявлением > 10 за час реакций ЭЭГ-активации (arousals) в сочетании с храпом или эпизодами затрудненного дыхания (по данным видео мониторинга), либо выявлялись нарушения дыхания, сопровождавшиеся наличием эпизодов десатурации менее 3% от базового уровня.
Распечатанные тренды Sa02 были проанализированы шестью специалистами (тремя технологами ПСГ и тремя врачами; все специалисты имели опыт работы в медицине сна не менее 2 лет). Эти специалисты, не имевшие какой-либо клинической информации о пациентах, подсчитывали количество событий десатурации >3% от базового уровня и рассчитывали индекс десатурации (среднее число эпизодов за час), после чего на основании величин ИД ставили клинический диагноз. Диагнозы были классифицированы с учетом величин ИД следующим образом: обструктивное апноэ сна тяжелой степени – ИД > 40); обструктивное апноэ сна средней тяжести – 20 < ИД < 40;. обструктивное апноэ сна легкой степени – 5 < ИД < 20; норма – ИД 2, не превышающие 3% от базового уровня. Так подсчет событий десатурации осуществлялся шестью специалистами, усредненный диагноз для каждого пациента формулировался следующим образом: каждый подсчитывавший события специалист использовал установленную шкалу для устанавливаемых диагнозов (ОАС тяжелой степени = 4; ОАС средней степени = 3; ОАС легкой степени = 2; СПРВДП = 1 и нормальное дыхание = 0). Итоговый диагноз для каждого пациента представляет собой среднее арифметическое диагнозов, поставленных специалистами. Результаты анализа сравнивались с финальными клиническими диагнозами, поставленными на основании анализа полисомнографических записей опытными врачами сомнологами.
Если данные о Sa02 оказывались недоступными из-за артефактов, плохой перфузии или смещения датчика с мочки уха в течение более трети времени записи, подсчитывающий специалист классифицировал данную запись как не интерпретируемую. Исследования, которые были признаны не интерпретируемыми более чем 3 специалистами, исключались из дальнейшего анализа.
Результаты
Тридцать одна запись из трехсот (10,3%) были исключены подсчитывающими специалистами. Финальные клинические диагнозы оставшихся 269 пациентов показаны в таблице 1.
Таблица 1. Клинические диагнозы 269 пациентов по данным полисомнографии.
| Клинический диагноз | Количество |
| Норма | 41 |
| СПРВДП | 65 |
| Легкая форма ОАС | 62 |
| ОАС средней степени | 23 |
| Тяжелая форма ОАС | 52 |
| ДЧС | 5 |
| ПДК | 13 |
| Нарколепсия | 4 |
| Парасомния | 2 |
| Синдром гиповентиляции, связанной с ожирением | 1 |
| Гиповентиляция после полиомиелита | 1 |
| Всего | 269 |
ДЧС: дыхание Чейна-Стокса; ПДК: периодические движения конечностей во время сна; ПСГ: полисомнография; ОАС: обструктивное апноэ сна; СПРВДП; синдром повышенной резистентности верхних дыхательных путей.
У 41 из 269 пациентов нарушения сна выявлены не были, у 65 был выявлен СПРВДП, у 137 – ОАС (от легкой до тяжелой степени), у 5 – дыхание Чейна Стокса, у 1 – синдром гиповентиляции, связанной с ожирением (СГО – непрерывная гиповентиляция во время сна с гиперкапнией, но без апноэ), у одного пациента была выявлена гиповентиляция после перенесенного полиомиелита, у 13 больных отмечались периодические движения конечностей во время сна (ПДК), у 4 – выявлена нарколепсия, а у 2 – парасомния.
В таблице 2 показаны результаты сравнительного анализа усредненных диагнозов, поставленных на основании изучения Sa02 у 269 пациентов, и финальных клинических диагнозов.
Таблица 2. Сравнительный анализ усредненных диагнозов, поставленных на основании изучения Sa02 шестью специалистами, и финальных клинических диагнозов по данным ПСГ.
| Диагноз по данным оксиметрии | № | Клинический диагноз по данным ПСГ | № |
| Норма | 66 | Норма | 30 |
| ПДК | 9 | ||
| Парасомния | 2 | ||
| Нарколепсия | 4 | ||
| СПРВДП | 20 | ||
| ОАС легкой степени | 1 | ||
| СПРВДП | 39 | Норма | 7 |
| ПДК | 3 | ||
| СПРВДП | 21 | ||
| ОАС легкой степени | 7 | ||
| ДЧС | 1 | ||
| ОАС легкой степени | 56 | Норма | 4 |
| ПДК | 1 | ||
| Гиповентиляция, связанная с ожирением | 1 | ||
| Гиповентиляция после полиомиелита | 1 | ||
| СПРВДП | 20 | ||
| ОАС легкой степени | 27 | ||
| ДЧС | 2 | ||
| ОАС средней степени | 44 | ОАС легкой степени | 22 |
| ОАС средней степени | 12 | ||
| ОАС тяжелой степени | 4 | ||
| ДЧС | 2 | ||
| СПРВДП | 4 | ||
| ОАС тяжелой степени | 64 | ОАС легкой степени | 5 |
| ОАС средней степени | 11 | ||
| ОАС тяжелой степени | 48 |
Примечание: В том случае, если у пациента выявлялось более одного диагноза, в качестве клинического диагноза указывалась ведущая причина избыточной дневной сонливости. СПРВДП диагностировался по критериям оксиметрии в случае наличия ИД < 5 и незначительных флуктуаций уровня насыщения крови кислородом. ПСГ: полисомнография; ПДК: периодические движения конечностей во время сна; ОАС: обструктивное апноэ сна; СПРВДП; синдром повышенной резистентности верхних дыхательных путей. ДЧС: дыхание Чейна-Стокса;
Из 66 пациентов, у которых на основании анализа Sa02 была диагностирована «норма» (отсутствие расстройств сна), только у 30 пациентов диагноз «норма» был подтвержден ПСГ-исследованием, у 1 выявлен ОАС легкой степени, у 20 – СПРВДП, у 9 – ПДК, у 4 – нарколепсия, а у 2 – парасомния. Таким образом, 36 случаев оказались ложно негативными. С другой стороны, из 203 пациентов, у которых был диагностирован ОАС или СПРВДП по данным оксиметрии, 11 оказались здоровыми (норма), а у 4 был выявлен синдром ПДК. Таким образом, 15 случаев оказались ложно позитивными. Чувствительность скрининга Sa02 для выявления связанных со сном нарушений дыхания (включая СПРВДП, ОАС, ДЧС, синдром гиповентиляции, связанной с ожирением и гиповентиляции у больных, перенесших полиомиелит) оказалась равной 90,0%, и специфичность оказалась равной 75%; положительная предиктивная значимость составила 92,6% и негативная предиктивная значимость – 45,5%. Пациенты с расстройством ПДК, нарколепсией и парасомниями были включены в этот расчет в качестве «здоровых», т.к. эти расстройства не оказывают влияние на уровень Sa02.
Таблица 3. Взаимосвязь клинических диагнозов и индивидуальных диагнозов, поставленных по данным оксиметрии шестью специалистами.
| Клинический диагноз | Процентная доля отдельных диагнозов | ||||
| Норма | СПРВДП | ОАС легкой степени | ОАС средней степени | ОАС тяжелой степени | |
| Норма | 76,4 | 12,5 | 10,8 | 0,3 | 0,0 |
| СПРВДП | 39,5 | 20,0 | 34,1 | 6,4 | 0,3 |
| СОАС легкой степени | 6,7 | 6,5 | 43,3 | 34,4 | 9,1 |
| СОАС средней степени | 0,0 | 0,0 | 4,3 | 55,8 | 39,9 |
| СОАС тяжелой степени | 0,0 | 0,0 | 1,0 | 9,9 | 89,1 |
Для каждого из пациентов, имевшего клинический диагноз, имелся и диагноз, поставленный на основании анализа результатов оксиметрии шестью специалистами. Сумма % в каждом ряду равна 100%. Для пациентов, которые по данным ПСГ-исследования, были признаны здоровыми, 76,4% индивидуальных диагнозов были корректными. Для пациентов с ОАС тяжелой степени 89,1% индивидуальных диагнозов были корректными. Процент верных диагнозов, поставленных на основании оксиметрии, для пациентов с СПРВДП, ОАС легкой и средней степени, оказался существенно ниже. ПСГ: полисомнография; СПРВДП: синдром повышенной резистентности верхних дыхательных путей; ОАС: обструктивное апноэ сна.
Чувствительность методики для выявления истинного ОАС (индекс апноэ-гипопноэ (ИАГ) > 5 по данным полисомнографии) при исключении СПРВДП, ДЧС, синдрома гиповентиляции на фоне ожирения или у больных, перенесших полиомиелит) составила 94,2%, а специфичность – 73,5%; положительная предиктивная значимость составила 78,7%, а негативная предиктивная значимость – 92,4%. Все пациенты с ОАС средней и тяжелой степени были определены по данным оксиметрии как больные с ОАС средней или тяжелой степени.
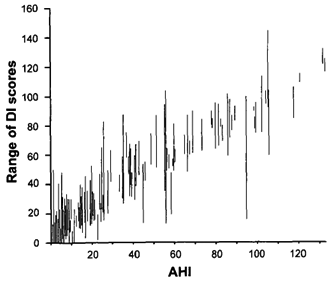
Рис. 1. Диапазон величин индекса десатурации (ИД) от максимума до минимума, подсчитанных шестью специалистами, для каждого из значений индекса апноэ-гипопноэ (по данным полисомнографии). Примечание: каждая линия представляет не отдельного пациента, а диапазон индексов апноэ-гипопноэ, к которому могут относиться несколько пациентов. Обратите внимание на то, что для некоторых пациентов с ОАС средней или тяжелой степени индивидуальные индексы десатурации были менее 20 событий в час. DI – индекс десатурации, AHI – индекс апноэ-гипопноэ, PSG – полисомнография.

Рис. 2. Вариабельность подсчитанных различными специалистами значений, представленная в виде стандартных отклонений/средних значений индексов десатурации для соответствующего значения ИАГ (по данным полисомнографии) для каждого пациента. Вариабельность была большей при ИАГ менее 10. DI – индекс десатурации; AHI – индекс апноэ-гипопноэ; PSG – полисомнография.
Для получения результатов, представленных выше, мы использовали усредненные данные шести подсчетов данных оксиметрии для каждого пациента. Так как для каждого из пациентов имелось шесть (основанных на оксиметрии) диагнозов, мы изучили взаимосвязь этих индивидуальных диагнозов с финальным диагнозом. В таблице 3 показаны результаты подсчетов ИД, сделанных каждым из специалистов, по отношению к каждому из клинических диагнозов пациентов (представлены в виде процентных долей). Мы установили, что % индивидуальных диагнозов по данным анализа Sa02 корреспондировали с финальными диагнозами (по ПСГ) следующим образом: норма – 76,4%; СПРВДП – 20%; ОАС легкой степени – 43,3%; ОАС средней степени – 55,8%; ОАС тяжелой степени – 89,1%. Это указывает на то, что поставить на основании мониторирования Sa02 диагнозы СПРВДП и ОАС легкой степени достаточно затруднительно, и имеет место существенная вариабельность диагнозов, поставленных подсчитывавшими специалистами, для этих пациентов.
Индекс десатурации рассчитанный отдельными подсчитывавшими специалистами, также имел большую степень вариабельности. На рисунке 1 показано, что диапазон ИД, рассчитанных каждым из специалистов (от меньшего до большего значений), был весьма вариабельным. Записи 51 пациента (18,9%) имели различия в величинах ИД более 20 между различными подсчитывавшими специалистами. Вариабельность подсчитанных различными специалистами значений, представленная в формате «стандартное отклонение/среднее значение» ИД, оказалась наибольшей в диапазоне ИД
Обсуждение
Скрининговый метод, позволяющий осуществлять отбор для последующих обследований пациентов, направленных в сомнологический центр связи с наличием избыточной дневной сонливости, должен быть эффективным и мало затратным. Результаты ряда исследований свидетельствуют о том, что домашняя оксиметрия может оказаться полезной при выявлении обструктивного апноэ сна. Недавно было показано, что синдром повышенной резистентности верхних дыхательных путей является важной причиной избыточной дневной сонливости. При этом синдроме могут проявляться, а могут и не проявляться легкие эпизоды десатурации; СПРВДП хорошо поддается лечению методом терапии постоянным положительным давлением (СРАР-терапии). Как нам известно, до настоящего времени не было проведено исследований, в которых изучалась бы эффективность применения домашней оксиметрии для скрининга данного синдрома, а также оценивался бы состав пациентов, направленных в лабораторию сна.
Таблица 4. Обзор предыдущих исследований.
| Исследование | Число больных (исключено) | Оксиметр | Датчик | Время ответа, сек. | Скорость забора данных, Гц | Кто подсчитывал | Падение Sa02, % | ИАГ | Чувстви-тельность, % | Специ-фичность, % |
| Douglas et al. | 200 (0) | Biox 3700 | Ухо | неизв. | неизв. | 1 | >4 | >5 | 67.0 | 91.7 |
| Series et al. | 240 (0) | Biox IVA | Палец | неизв. | 0,5 | неизв. | не определено | >10 | 98.2 | 47.7 |
| Shoohs et al. | 56 (1) | MESAM 4 | Палец | неизв. | неизв. | комп. | >3 | >10 | 97 | 92 |
| Farney et al. | 54 (искл.) | BIOX IIA | Ухо | неизв. | неизв. | 2 | >4 | само апноэ | 80 | 71 |
| Williams et al. | 40 (4) | Biox 3700 IV, Nellcor N100 | неизв. | неизв. | 0,17 | неизв. | >4 и <90% | >10 | 75 | 100 |
| Cooper et al. | 41 (6) | Biox II A | Ухо | неизв. | неизв. | 2 | >5 (и >15, >25) | >5 | 60 | 95 |
| Gyulay et al. | 98 (0) | Biox 3700 | неизв. | неизв. | 0,08 | неизв. | >3 (и >2, >4) | >15 | 51 | 90 |
| Pepin et al. | 26 (0) | Biox 3700 | Палец | неизв. | 0,08 | комп. | порог дельта | >5 | 75 | 86 |
| Decker et al. | 16 (10-20% данных) | Criticare 501+ | Палец | неизв. | неизв. | неизв. | средний уровень Sa02 и 50% времени < значения Sa02 | неизв. | неизв. | неизв. |
| Rauscher et al. | 116 (0) | Pulsox 7 | неизв. | неизв. | неизв. | 1 | Циклические осцилляции >30 мин | >10 | 94 | 62 |
| Наши данные | 300 (31) | Biox 3740 | Ухо | 3 | 2 | 6 | >3 | >5 | 90.0 | 75.0 |
ИАГ: индекс апноэ гипопноэ; комп: анализировалось при помощи компьютера.
Большинство авторов сходятся во мнении, что все оксиметры являются одинаково надежными. Известно, что динамический ответ оксиметра может варьировать, что в свою очередь зависит от того, какой прибор и какой датчик были использованы. Нарушения дыхания во время сна обычно сопровождаются динамическими изменениями уровня Sa02, поэтому для точного выявления событий десатурации потребуется оборудование с максимально быстрым ответом. Warley и соавт. установили, что задержка ответа (показаний прибора) составила 23.6 при применении датчика на пальце и 9.8 секунд при использовании ушного датчика. Продолжительность задержки имела корреляционную связь с частотой сердечных сокращений. Само по себе наличие задержки может и не представлять проблемы; вместе с тем, рад исследователей показали, что различные виды датчиков и их различное размещение, а также наличие брадикардии, могут существенно повлиять на точность некоторых оксиметров.
Применение низкой частоты забора данных может привести к тому, что характеристики зарегистрированной кривой Sa02 могут существенно отличаться от реальной кривой, т.к. многие пики и провалы могут быть пропущены. Например, если оксиметр Biox 3700 сохранял в памяти только минимальные значения Sa02 каждые 12 секунд, кривая, полученная из памяти устройства, существенно отличалась по своему внешнему виду от оригинальной кривой; несмотря на то, что минимальные значения Sa02 были зафиксированы правильно, максимальное восстановление оставалось недооцененным. Таким образом, при применении данных устройств для домашней оксиметрии, кривая Sa02 из памяти устройства может оказаться неверной.
В таблице 4 представлены сводные данные по опубликованным результатам исследований, в которых анализировалась проблема применимости оксиметрии для выявления апноэ сна. В четырех исследованиях использовались датчики на пальце, и в трех исследованиях – ушные датчики. Во всех исследованиях авторами не указано время ответа (задержки) показаний оксиметра. В четырех публикациях была указана частота (скорость) забора данных, при этом в трех из них интервалы забора данных были очень продолжительными (0,2 Гц и 0,08 Гц). Большой разброс показателей чувствительности и специфичности между указанными публикациями может быть обусловлен данными техническими факторами и различными критериями определения минимальных значений ИАГ и изменений Sa02.
Другая проблема, связанная с применением оксиметрии, заключается в том, что на качество сигнала влияют различные факторы, такие, как движения пациента, контакт датчика с кожей и состояние местного кровотока. Датчик может сместиться с пальца (уха) пациента во время исследования. Тридцать одна запись (10,3%) в нашем исследовании были исключены из анализа из-за неадекватных данных или присутствия артефактов. Сходные % неадекватных данных были указаны авторами и других исследований (Табл. 4). Большинство авторов не уделяют большого внимания данной проблеме. Наши записи были получены во время контролируемых ПСГ-исследований, когда технолог должен был обеспечивать качество сигналов, и этот вариант представляет собой наиболее идеальный тип исследований. Мониторирование показателей оксиметрии в домашних условиях может сопровождаться большим риском неадекватных исследований. Это свидетельствует о том, что не менее 10% исследований оксиметрии в домашних условиях могут потребовать проведения повторного исследования.
У некоторых пациентов с СПРВДП по данным исследователей выявлялись периодические флуктуации уровня Sa02. Мы использовали данный критерий при диагностике СПРВДП; вместе с тем, у 20 из 66 наших пациентов (30,3%), которые по данным оксиметрии были отнесены к здоровым, был выявлен СПРВДП по данным ПСГ-исследования в сочетании с видеомониторингом, показавшими наличие громкого храпа, затрудненного дыхания и реакций ЭЭГ-активации. У данных больных отсутствовали визуально определяемые периодические флуктуации Sa02. Таким образом, пациенты с СПРВДП, наряду с пациентами с расстройством ПДК или нарколепсией (не оказывающими влияние на уровень Sa02), могут оказаться не выявленными при помощи домашней оксиметрии.
В большинстве из проанализированных выше исследований диагноз ставился одним или двумя подсчитывавшими специалистами. Вместе с тем, мы выявили существенный разброс в постановке диагнозов и величинах ИД между подсчитывающими специалистами, особенно, если ИД был меньше 10. Таким образом, если ИД у пациента <10, риск неправильной диагностики увеличивается. Это может быть дополнительной причиной затруднений при диагностике СПРВДП при помощи оксиметрии.
Философия скрининга заключается в том, что он должен быть очень чувствительным (почти нет ложно негативных результатов). Ценой подобной высокой чувствительности может быть существенная частота ложно положительных результатов. Проведенные в последующем высоко специфичные методы исследования позволят поставить точный диагноз и обеспечат то, чтобы людям, не имеющим патологии, лечение не проводилось, а больные, имеющие патологию, получали адекватное лечение.
Наши результаты свидетельствуют о том, что скрининговые исследования с применением изолированной оксиметрии могут не принести пользы при диагностике ряда вариантов нарушений дыхания во сне, включая СПРВДП, т.к. чувствительность и специфичность этого метода является недостаточно высокой для скринингового метода. Таким образом, в чем же заключается в настоящее время роль оксиметрии? Так как тяжелая гипоксемия является потенциально угрожающим жизни состоянием, оксиметрия может быть использована для выделения приоритетных групп пациентов, требующих неотложного лечения. Например, результаты нашего исследования показали, что оксиметрия позволила выявить большинство больных с апноэ сна средней и тяжелой степени. Комбинация данных оксиметрии с другой информацией (результатами анкетирования, данными о громкости храпа, паттернах дыхания может оказать существенную помощь при клинической оценке больного, однако роль подобных комбинированных тестов должна быть тщательно оценена (в том числе их влияние на процесс принятия клинических решений). Williams и соавт. показали, что анализируя данные оксиметрии вместе с клиническими параметрами (включая симптомы, индекс массы тела и уровень АД) существенно повышает чувствительность методики.
Данные о возможности скрининга расстройств сна при помощи оксиметрии являются противоречивыми. Полученные нами результаты свидетельствуют о том, что применение оксиметрии в качестве инструмента скрининга было связано с определенными проблемами из-за того, что многие из исследований были не адекватными, часто отмечалась несогласованность в интерпретации результатов исследований, и пациенты с потенциально излечимыми расстройствами могли быть пропущены. Если пациент страдает от избыточной дневной сонливости, ему должен быть поставлен диагноз. Негативные результаты скрининга у такого пациента не помогают ни пациенту, ни врачу, так как не позволяют избежать последующего дополнительного обследования. Аналогично, положительные результаты скрининга, также требуют проведения последующего обследования (ПСГ для подтверждения и/или ПСГ с титрацией режима СРАР).
Проводя итоговый анализ, специалист должен принять решение относительно клинической роли оксиметрии, также как и других скрининговых методик и других исследований. Что делать в случае позитивного результата скрининга? Что делать при негативном результате? Если ответ на оба эти вопроса звучит одинаково, данный тест в действительности не помогает при принятии решений.
Мы пришли к выводу о том, что изолированная домашняя оксиметрия не является полезным методом исследований при обследовании пациентов с избыточной дневной сонливостью.